新冠核酸检测实验室建设要求,先了解这6点
RT-PCR是检测新型冠状病毒核酸最广泛、最准确的筛选和确认方法。大规模的核酸检测将不可避免地引起相关机构和单位重视建立标准化的临床PCR实验室。相关建设问题可咨询020-29038089。
.
一、新冠核酸检测PCR实验室建设依据
新型冠状病毒实验室生物安全指南(第二版)
GB19489-2008《实验室生物安全通用要求》
GB50346-2011《生物安全实验室建筑技术规范》
WS233-2017《病原微生物实验室生物安全通用准则》
《临床基因扩增实验室管理暂行办法》卫生部
《医疗机构临床基因扩增检验实验室管理办法》卫办医政发【2010】194号
《医疗机构临床基因扩增检验实验室工作导则》
二、初步了解PCR实验室
如何避免污染是临床基因扩增实验室设计的关键问题。因此,实验室的布局、空调通风系统设计、风量控制等都是围绕这一核心问题展开的。
(1)现场要求高。需要标准的四区分离和气流控制:试剂制备、样品制备、PCR扩增检测和扩增产物检测。每个独立的实验区都有一个缓冲区。同时,每个区域均采用气压调节,使试剂和样品在整个PCR实验过程中不受气溶胶污染,减少扩增产物对人和环境的污染。机械连锁不锈钢传递窗确保试剂和样品在转移过程中不受污染(人员分流)。
(2)人员要求高。进入PCR实验室,需要接受基础理论、实验原理、标准操作、质量保证、注意事项等方面的标准培训,并取得PCR工作证。
(3)高检测风险。在检测过程中,由于样品盖的打开、核酸提取的振动和离心作用,可能产生气溶胶,存在感染的风险。
(4)防护要求高。个人防护必须按照生物安全三级实验室的个人防护要求进行。
三、新冠核酸检测实验室设计参数(供参考)
| 区域 | 洁净度等级 | 最小换气次数(次/小时) | 与室外方向上相邻相通房间最小压差(Pa) | 温度(℃) | 相对湿度(%) | 风速(m/s) | 噪声dB(A) |
| 试剂储存和准备区 | 8 | 12 | +10 | 18~26 | 40-60 | ≤0.15 | <60 |
| 样本制备区 | 8 | 15 | -10 | 18~26 | 40-60 | ≤0.15 | <60 |
| 核酸扩增区 | 8 | 15 | -15 | 18~26 | 40-60 | ≤0.15 | <60 |
| 产物分析区 | 8 | 15 | -20 | 18~26 | 40-60 | ≤0.15 | <60 |
| 缓冲间 | - | 6 | 0 | 18~26 | 40-60 | —— | <60 |
| PCR专用走廊 | - | 6 | 5 | 18~26 | 40-60 | —— | <60 |
四、 新冠核酸检测实验室建设的几个关键点
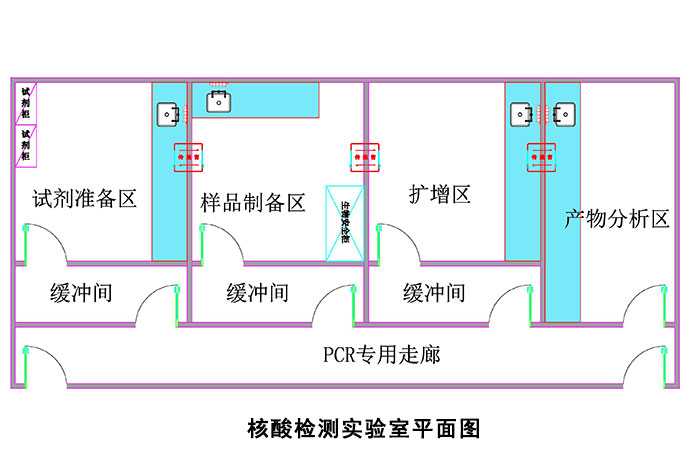
(1)平面布局:不论是组合式还是分散式布置的PCR实验室,各功能房间均宜设置独立缓冲间
(2)区域空气流向:为避免交叉污染,PCR实验室空气流向必须严格遵循单一方向进行,即只能从试剂贮存和准备区→标本制备区→扩增反应混合物配制和扩增区→扩增产物分析区。
(3)通风空调:为避免交叉污染,各功能用房内空气不能掺混。混合式PCR实验室应采用新风直流空调系统,当采用新风系统有困难时,各区域的空气只能在自己的房间内循环。
(4)生物安全:按照新型冠状病毒实验室生物安全指南(第二版)的规定,2019-nCoV病原体暂按照第二类病原微生物进行管理,则样本植被区宜为负压或加强型P2实验室,核酸操作应在生物安全柜内进行。
关键技术措施包括:
*绝对负压(避免室内潜在污染外泄)
*气流组织(室内定向流,从低污染风险区流向高污染风险区)
*排风无害化处理(高效过滤、高空排放)
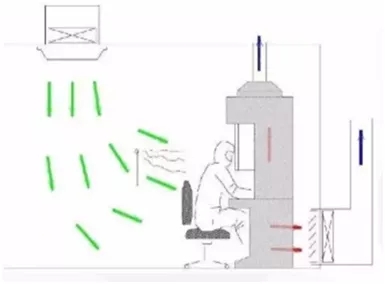
五、新冠核酸检测实验室气流组织建议
(1)气流组织宜采用上送下排,送风口和排风口布置应使室内气流停滞的空间降低到最小程度。
(2)在生物安全柜操作面或其他有气溶胶操作地点的上方附件不得设送风口
(3)高效过滤器排风口应设在室内被污染风险最高的区域,单向布置,不得有障碍;
(4)不能以回(排)风夹墙代替排风直管,排风高效过滤装置与排风总管的连接必须全部是实体风管。
六、新冠核酸检测实验室装饰装修
核酸检测实验室有设计理念、装修要求、净化空调系统、通风、自控、工艺设备等几个关键点。

要求:
1.墙面:光洁、不产尘积尘、耐腐蚀,易清洁消毒、无缝隙;
2.地面:防静电、耐腐蚀、无缝隙、无渗漏;
3.阴阳角:均用圆弧角密封处理;
4.门:必须设置自动互锁(机械或电子);

1.避免交叉污染,采用全新风空调系统;
2.样品制备区严格按照BSL-2设计施工;
3.排风系统全部按照要求采用高效过滤器净化;
4.气流组织:采用上送下排形式;
5.压力梯度控制通过微压差计及精密自控系统控制;
6.实验室入口处显示房间内各项指标参数,并设置偏离报警;
工艺设备
1.实验台下部均留空,无死角;
2.全部采用不锈钢304制作;
3.样品制备区生物安全柜:BSC-||-B2型;
4.样品制备区设置洗眼装置,必要时应有应急喷淋装置;
5.非接触式操作理念(感应式水龙头、感应式自动门、互锁传递窗等);
实验室建设涉及到材料选择、稳定性、精度控制等多个技术和知识领域。不同的实验室由于试验样品和试验方法的不同,对实验室建设有不同的要求。可以说有很多不同之处。一个完善的实验室在分析检测中起着重要的作用,对保证实验室工作人员的健康也起着重要的作用。





